Introducción a la Tomografía Computada (TC)
Fundamentos para comprender la imagen tomográfica
*Este es un artículo básico para estudiantes de Medicina y otras Ciencias de la Salud.
- Introducción a la Tomografía Computada (TC)
- Introducción
- ¿Qué problema resuelve la TC frente a la radiografía?
- Componentes del tomógrafo y adquisición: de “girar y medir” a “reconstruir y ver”
- Cómo se forma la imagen en TC
- 1) Atenuación: lo que el detector realmente mide
- 2) Proyecciones y sinograma: muchas mediciones para reconstruir un corte
- 3) Reconstrucción: la computadora hace el “trabajo pesado”
- 4) Vóxel, píxel y volumen parcial: el “promedio” que a veces engaña
- Unidades Hounsfield (HU): el idioma numérico de la TC
- ¿Por qué necesitamos ventanas?
- Ejemplos de ventanas frecuentes (números típicos)
- Planos y reconstrucciones: del corte axial a la visión volumétrica
- TC helicoidal y multicorte: por qué cambió la práctica clínica
- Radiación ionizante en TC: riesgos, indicadores y qué puede hacer el médico solicitante
- Resumen
- Puntos clave
- Referencias
- Artículos relacionados
Introducción
La tomografía computada (TC) es, en esencia, una forma de “radiografía por partes”: en lugar de proyectar toda la anatomía en una sola imagen (con superposición), la TC reconstruye cortes del cuerpo a partir de múltiples mediciones de atenuación de rayos X tomadas desde distintos ángulos.
En este post vas a entender cómo se forma la imagen sin entrar en matemática pesada, cómo se traduce la atenuación en Unidades Hounsfield y por qué necesitamos ventanas para ver bien tejidos diferentes. También revisaremos las modalidades de visualización (planos, MPR, MIP, 3D) y el punto que nunca hay que olvidar: la exposición a radiación ionizante y cómo se expresa en los indicadores de dosis que reportan los equipos.
¿Qué problema resuelve la TC frente a la radiografía?
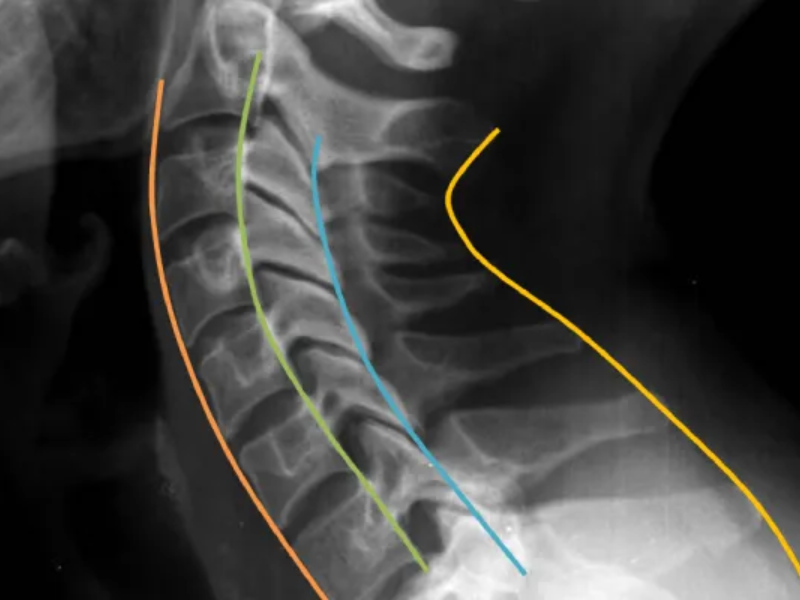
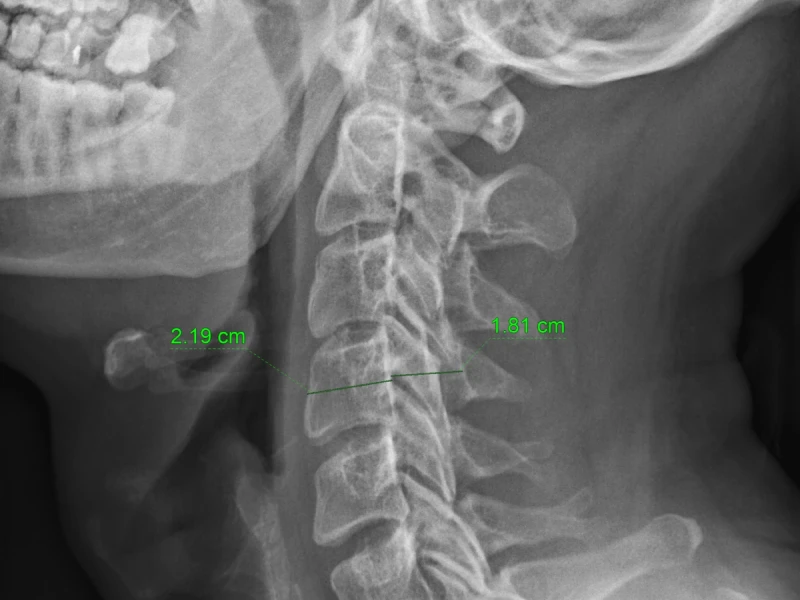
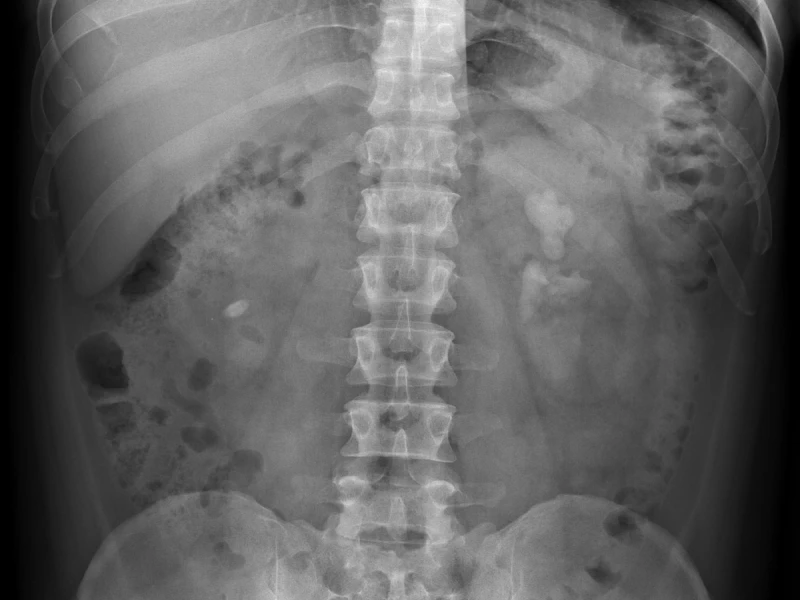
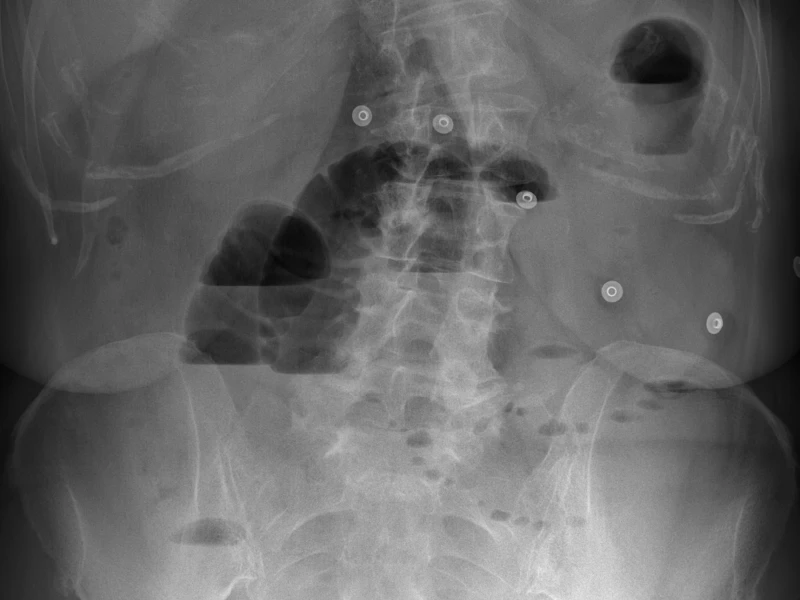
En radiografía convencional, todo lo que atraviesa el haz queda “apilado” en la misma imagen. La TC nació para superar limitaciones prácticas de la radiografía, especialmente la superposición, la baja diferenciación de tejidos blandos y la dificultad para cuantificar densidades de forma reproducible.
Ese último punto es clave: la TC asigna un valor numérico a cada pequeño volumen de tejido (vóxel), lo que permite medir atenuación y comparar entre estudios, ventanas y protocolos (con matices que veremos).
Componentes del tomógrafo y adquisición: de “girar y medir” a “reconstruir y ver”
Componentes básicos (lo que conviene tener en mente)
Un tomógrafo incluye, como mínimo: tubo de rayos X, gantry con detectores, computadora y el sistema de movimiento de la mesa. En el trayecto del haz aparecen elementos que afectan calidad y dosis: filtro (quita fotones de baja energía), colimación (limita dispersión y reduce dosis) y la matriz de detectores (convierte rayos X a señal eléctrica).
Adquisición “axial” y adquisición “helicoidal”
- En la adquisición axial clásica (step-and-shoot), el equipo adquiere un corte, la mesa avanza y se repite.
- En la tomografía helicoidal, el tubo rota de manera continua mientras la mesa se desplaza: el haz describe una trayectoria en hélice y se obtiene una adquisición volumétrica.
Esa adquisición volumétrica es la base práctica de muchas reconstrucciones multiplanares y 3D que hoy damos por sentadas.
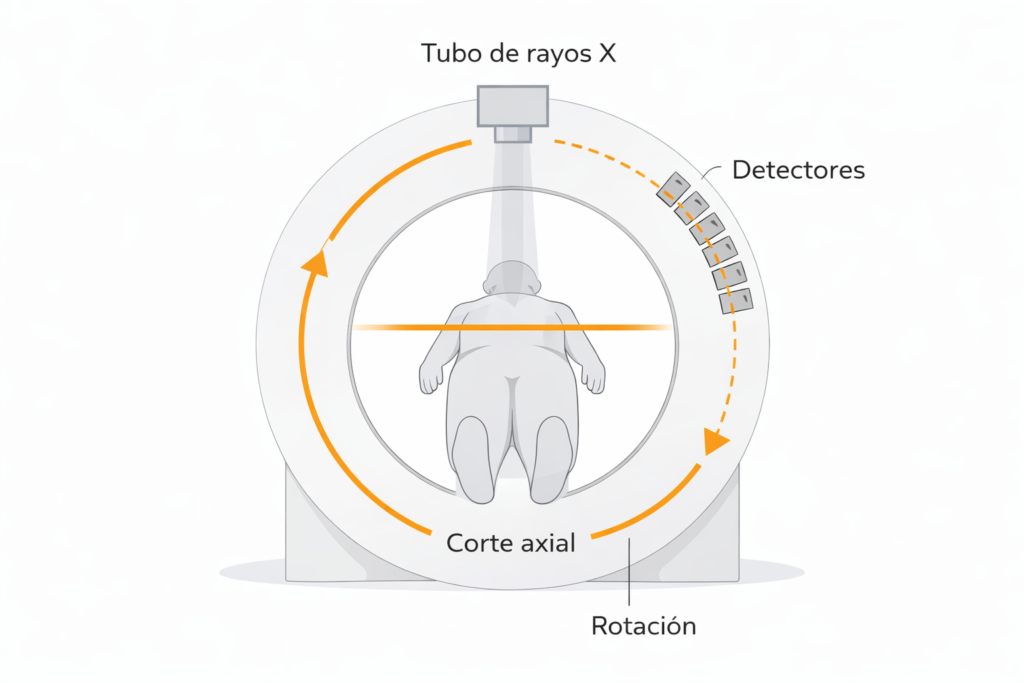
Principio de la tomografía computada. El tubo de rayos X y los detectores rotan alrededor del paciente, obteniendo múltiples mediciones de atenuación que la computadora reconstruye para formar un corte axial sin superposición de estructuras.
Cómo se forma la imagen en TC
1) Atenuación: lo que el detector realmente mide
Cada tejido atenúa (absorbe y dispersa) el haz de rayos X según su composición y espesor. Esa idea se formaliza con la ley de atenuación, y es la base para entender por qué aire, grasa, agua, músculo y hueso se ven distintos.
2) Proyecciones y sinograma: muchas mediciones para reconstruir un corte
En TC no se “fotografía” un corte directamente. Se miden proyecciones desde múltiples ángulos: cada una es una señal 1D (intensidades) y, apiladas, forman una matriz conocida como sinograma. Tras la reconstrucción, obtenemos una imagen 2D donde cada píxel representa la atenuación estimada del vóxel correspondiente.
3) Reconstrucción: la computadora hace el “trabajo pesado”
El problema central es asignar una atenuación a cada vóxel a partir de esas proyecciones. Existen métodos analíticos (como retroproyección filtrada) e iterativos; en la práctica moderna predominan técnicas de reconstrucción iterativa en muchos equipos por su impacto en ruido y dosis.
Idea clínica útil: si entendés que la imagen depende de cómo se adquiere y cómo se reconstruye, se vuelve más fácil interpretar por qué cambian el ruido, el detalle fino, o aparecen artefactos.
4) Vóxel, píxel y volumen parcial: el “promedio” que a veces engaña
La TC trabaja con vóxeles (volúmenes). Si dentro de un mismo vóxel hay dos tejidos muy distintos, la atenuación se promedia y puede simular lesiones o borrar bordes: es el efecto de volumen parcial.
Unidades Hounsfield (HU): el idioma numérico de la TC
Los números CT o Unidades Hounsfield (HU) normalizan la atenuación tomando al agua como referencia (agua ≈ 0 HU). Una definición habitual expresa el HU como una comparación entre el coeficiente de atenuación del tejido y el del agua.
Valores orientativos clásicos que conviene memorizar (aprox.):
- Aire: ~ −1000 HU
- Grasa: ~ −70 a −90 HU
- Tejidos blandos: valores positivos bajos (p. ej., +30 a +70 HU)
- Hueso: cientos de HU (p. ej., alrededor de +500 HU o más según el tipo y la medición)
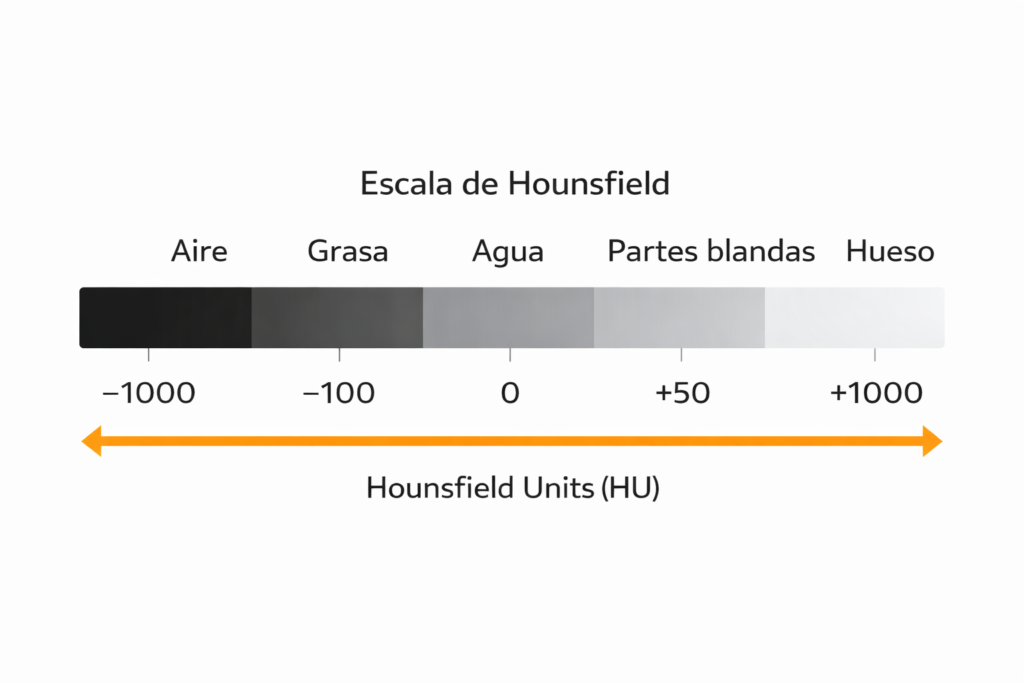
Escala de Hounsfield. Representa los valores de atenuación medidos en tomografía computada. El aire se aproxima a −1000 HU, el agua a 0 HU y el hueso presenta valores positivos elevados. Esta escala permite cuantificar densidades y diferenciar tejidos en las imágenes de TC.
¿Por qué necesitamos ventanas?
El monitor no puede mostrar “toda” la escala de HU con detalle útil a la vez. La ventana define qué rango de HU se asigna a grises visibles:
- Window level (WL): punto medio del rango.
- Window width (WW): amplitud del rango.
Dos reglas prácticas:
- WW más angosta → más contraste (pero saturás antes blancos/negros).
- Ajustá el WL cerca del tejido que querés evaluar (pulmón “bajo”, hueso “alto”, tejidos blandos intermedio).
Ejemplos de ventanas frecuentes (números típicos)
Los valores varían por estación de trabajo y preferencia, pero como orientación:
- Tejidos blandos (abdomen): WW ~350–400 / WL ~40
- Pulmón: WW ~1400 / WL ~ −500
- Hueso: WW ~1500 / WL ~300
- Cerebro: WW ~80 / WL ~40
Errores comunes del no especialista: “No hay lesión” cuando en realidad la ventana no es la adecuada; o confundir hiperdensidad por ventana ósea con calcificación/hemorragia sin correlación clínica ni ventana correcta.
Planos y reconstrucciones: del corte axial a la visión volumétrica
Planos ortogonales y MPR
Aunque el corte axial sea la adquisición “clásica”, hoy es rutina reconstruir en coronal y sagital (y oblicuos) mediante reconstrucción multiplanar (MPR). Estas reconstrucciones mejoran mucho la evaluación anatómica y la lectura, sobre todo en regiones complejas.
Para que MPR sea realmente útil, ayuda contar con resolución similar en todos los ejes (resolución isotrópica), algo que se favorece con cortes finos y adquisiciones volumétricas modernas.
MIP y 3D (qué hacen y para qué sirven)
- MIP (maximum intensity projection): proyecta, a lo largo de un volumen elegido, los vóxeles de mayor atenuación. Es especialmente útil para vasos opacificados con contraste, calcificaciones y algunos patrones pulmonares (según el caso).
- 3D / volume rendering: usa todo el volumen para crear representaciones tridimensionales (útil en vascular, trauma, planificación, etc.).
[Nota de alcance] Estas técnicas se apoyan en el concepto de adquisición volumétrica y posprocesamiento en estaciones de trabajo, y su utilidad clínica creció con la TC helicoidal/multidetector.
Kernel (filtro de reconstrucción) y grosor de corte: la pareja que cambia el “aspecto” de la imagen
En términos simples:
- Un kernel más “agudo” aumenta resolución espacial pero incrementa ruido.
- El grosor de corte controla la resolución en el eje longitudinal.
Esto explica por qué el mismo estudio puede “verse distinto” según la serie (pulmón con cortes finos vs abdomen con cortes más gruesos, por ejemplo).
TC helicoidal y multicorte: por qué cambió la práctica clínica
Hélice (pitch): rapidez, cobertura y dosis/calidad
En helicoidal, un parámetro central es el pitch, que relaciona el avance de la mesa por rotación del tubo con el grosor/colimación del haz.
Conceptualmente:
- Mayor pitch → barrido más rápido y menor dosis, a costa de potencial pérdida de calidad (dependiendo del equipo, reconstrucción y protocolo).
Multidetector (multicorte): más filas de detectores, más volumen, más 3D “real”
El paso a TC multidetector (varias filas de detectores) mejoró resolución espacial/temporal y permitió cubrir más anatomía en menos tiempo, facilitando exploraciones en apnea única y ampliando aplicaciones (incluidas angiografías por TC).
Radiación ionizante en TC: riesgos, indicadores y qué puede hacer el médico solicitante
Lo importante: beneficio diagnóstico vs exposición
La TC usa radiación ionizante. En radioprotección clínica, la idea central es: justificación (hacer el estudio cuando aporta) y optimización (usar la menor dosis razonable para responder la pregunta clínica).
Por qué no se mide “dosis efectiva” paciente por paciente
En TC (como en otras técnicas), no es posible medir directamente la dosis efectiva o en órganos de un paciente particular; se trabaja con modelos y mediciones en fantomas para estimar magnitudes útiles.
Los dos números que vas a ver en el reporte del equipo: CTDIvol y DLP
- CTDI (índice de dosis en TC): indicador estandarizado de la salida de radiación en un corte.
- CTDIvol: incorpora el pitch y se usa mucho como indicador de dosis para un protocolo.
- DLP (producto dosis-longitud): aproxima la energía total impartida y se correlaciona (con limitaciones) con riesgo; en forma práctica: DLP = CTDIvol × longitud escaneada.
Estrategias típicas de reducción de dosis (conceptuales)
- Modulación de mAs: reduce corriente del tubo en regiones de menor atenuación; el cambio de mAs impacta linealmente la dosis.
- Ajuste de pitch: a salida constante, aumentar pitch puede disminuir dosis; bajarlo puede aumentarla.
- Ajuste de kV: cambia la dosis de forma no lineal y depende del tamaño/peso; puede mejorar relación contraste-ruido en escenarios seleccionados.
Checklist breve para el médico no radiólogo (antes de pedir una TC)
- ¿La TC responde una pregunta clínica concreta o hay alternativa sin ionizantes (p. ej., US/RM) adecuada?
- ¿Hay estudios previos recientes que eviten repetir?
- ¿La región a escanear está bien delimitada (para no “alargar” el barrido)? → impacta DLP.
- ¿Se necesita contraste yodado? (Esto se profundiza en el post de medios de contraste; aquí alcanza con reconocer que es parte del protocolo).
Resumen
La TC reconstruye cortes a partir de múltiples proyecciones de rayos X y traduce la atenuación de cada vóxel en Unidades Hounsfield, lo que permite ajustar ventanas para visualizar mejor distintos tejidos. Con adquisiciones volumétricas (helicoidal y multicorte) es posible obtener reconstrucciones MPR, MIP y 3D que mejoran la lectura según la pregunta clínica. Como usa radiación ionizante, conviene conocer CTDIvol y DLP, y aplicar criterios de justificación y optimización.
Puntos clave
- La TC no “fotografía” un corte: mide proyecciones y luego reconstruye la imagen.
- Cada vóxel recibe un valor en Unidades Hounsfield; agua ≈ 0 HU y aire ≈ −1000 HU.
- Las ventanas (WW/WL) determinan el rango de HU visible y, por lo tanto, el contraste útil.
- MPR (coronal/sagital) y otras reconstrucciones dependen de la adquisición volumétrica y cortes finos.
- El pitch en helicoidal afecta cobertura, calidad y dosis (en general, mayor pitch reduce dosis con posibles trade-offs).
- En el reporte de dosis, CTDIvol y DLP son los indicadores más usados; DLP = CTDIvol × longitud escaneada.
Referencias
- European Society of Radiology. ESR Modern Radiology eBook: Computed Tomography (2024). DOI: 10.26044/esr-modern-radiology-04.
- Ramírez JC, Arboleda C. Tomografía computarizada por rayos X: fundamentos y actualidad. Revista Ingeniería Biomédica.
- Calzado A, Geleijns J. Tomografía computarizada. Evolución, principios técnicos y aplicaciones. Rev Fis Med. 2010.
- Hernández Muñiz S, et al. Introducción a la tomografía computarizada. Rev Esp Med Nucl. 2006;25(3):206–216.
- Del Bosque Patoni C, et al. Principios básicos y aplicaciones clínicas de la tomografía computada helicoidal multicorte. Acta Médica Grupo Ángeles. 2006.
- Andisco D, Blanco S, Buzzi AE. Dosimetría en tomografía computada. Rev Argent Radiol. 2014;78(3):156–160.
- Gibbs JM, et al. Lines and Stripes: Where Did They Go?—From Conventional Radiography to CT. Radiographics. 2007.